Graf KV62, gelegen in de Vallei der Koningen in Egypte, is een koninklijk Egyptisch graf met daarin de mummie van Toetanchamon.
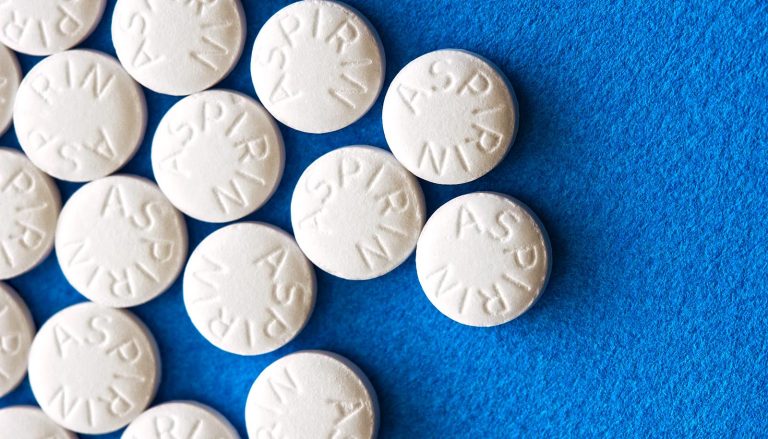
Bijna een eeuw lang riep de naam Aspergillus flavus verhalen op over mysterie, ziekte en dood. Na de opening van het graf van Toetanchamon in 1922 werd Aspergillus flavus aangewezen als de onzichtbare boosdoener achter de zogenaamde “Farao’s vloek”.
Jane Goodall: “Wat je doet maakt een verschil en je moet beslissen welk verschil je wilt maken”. Steun ons werk, bescherm de planeet.
Vandaag de dag is diezelfde schimmel, die ooit gevreesd werd bij archeologische opgravingen, door de wetenschap getransformeerd in een therapeutische hoop voor duizenden patiënten. Een interdisciplinair team onder leiding van onderzoekers van de Universiteit van Pennsylvania heeft moleculen van deze giftige schimmel ontdekt en veranderd in verbindingen die kankercellen kunnen vernietigen met een werkzaamheid die vergelijkbaar is met door de FDA goedgekeurde medicijnen tegen leukemie.
Deze buitengewone ontdekking, onlangs gepubliceerd in Nature Chemical Biology, toont eens te meer aan dat het schimmelrijk, dat zo vaak genegeerd of gevreesd wordt, een chemisch arsenaal verbergt met een onontgonnen therapeutisch potentieel.
“Schimmels gaven ons penicilline,” herinnert Sherry Gao, professor chemische technologie en bio-engineering aan Penn en hoofdauteur van het onderzoek, zich. “Deze resultaten laten zien dat er nog veel medicijnen te ontdekken zijn in natuurlijke producten.”
Aspergillus flavus
Het verhaal van Aspergillus flavus begint in de diepten van koninklijke graven en gaat verder in moderne laboratoria. Na de mysterieuze dood van een aantal archeologen die betrokken waren bij de opening van het graf van Toetanchamon, raakten theorieën over sporen uit de oudheid in een stroomversnelling.
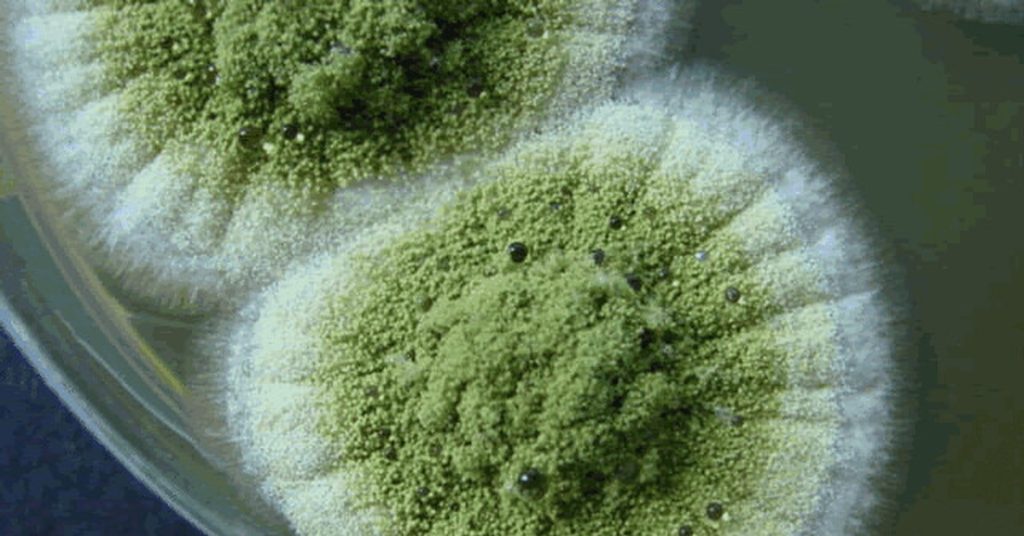
Tientallen jaren later deed zich een soortgelijk incident voor in Polen: van de twaalf wetenschappers die het graf van koning Casimir IV betraden, stierven er tien binnen een paar weken. De onzichtbare boosdoener: dezelfde schimmel, waarvan de giftige metabolieten dodelijke longinfecties kunnen veroorzaken bij mensen met een verminderde immuniteit.
Maar nu is het verhaal op zijn kop gezet. In plaats van een bedreiging zou A. flavus een redder in nood kunnen worden.
Het team van wetenschappers ontdekte een type verbinding genaamd RiPP’s, kort voor ribosomaal gesynthetiseerde en post-translationeel gemodificeerde peptiden. Deze moleculen, geproduceerd door het cellulaire ribosoom en vervolgens chemisch gemodificeerd, zijn voornamelijk waargenomen in bacteriën, maar bijna nooit in schimmels.
Het feit dat ze zijn gevonden in A. flavus is een doorbraak. “De zuivering van deze verbindingen is een ingewikkeld proces, maar het is juist deze complexiteit die ze zo’n opmerkelijke bioactiviteit geeft,” legt Qiuyue Nie, eerste auteur van het artikel, uit.
De onderzoekers noemden deze nieuwe moleculen asperigimycines, naar de schimmel waarvan ze afkomstig zijn. Verrassend genoeg vertoonden twee van de geëxtraheerde varianten anti-leukemische activiteit zonder verdere modificatie. Een andere variant, versterkt met een lipide die lijkt op die in koninginnengelei van bijen, vertoonde een werkzaamheid die vergelijkbaar was met die van klassieke geneesmiddelen zoals cytarabine en daunorubicine.
Deze lipidemodificatie verhoogde niet alleen de werkzaamheid van asperigimycine, maar onthulde ook een cruciaal cellulair mechanisme. Door specifieke genen in leukemiecellen aan of uit te zetten, ontdekten de wetenschappers dat één ervan, SLC46A3, een vitale rol speelde: het zorgde ervoor dat de verbindingen via lysosomen in de celkern terechtkwamen. “Het is als een poort,” zegt Nie.
Deze bevinding zou implicaties kunnen hebben die verder gaan dan dit onderzoek en de toegang van andere, vergelijkbare therapeutische verbindingen kunnen vergemakkelijken.
Leukemiekankers
Bij verdere tests stelden de onderzoekers vast dat asperigimycines de vorming van microtubuli blokkeerden, sleutelstructuren bij de celdeling. Dit is vooral relevant bij kankers zoals leukemie, waar cellen zich ongecontroleerd vermenigvuldigen.
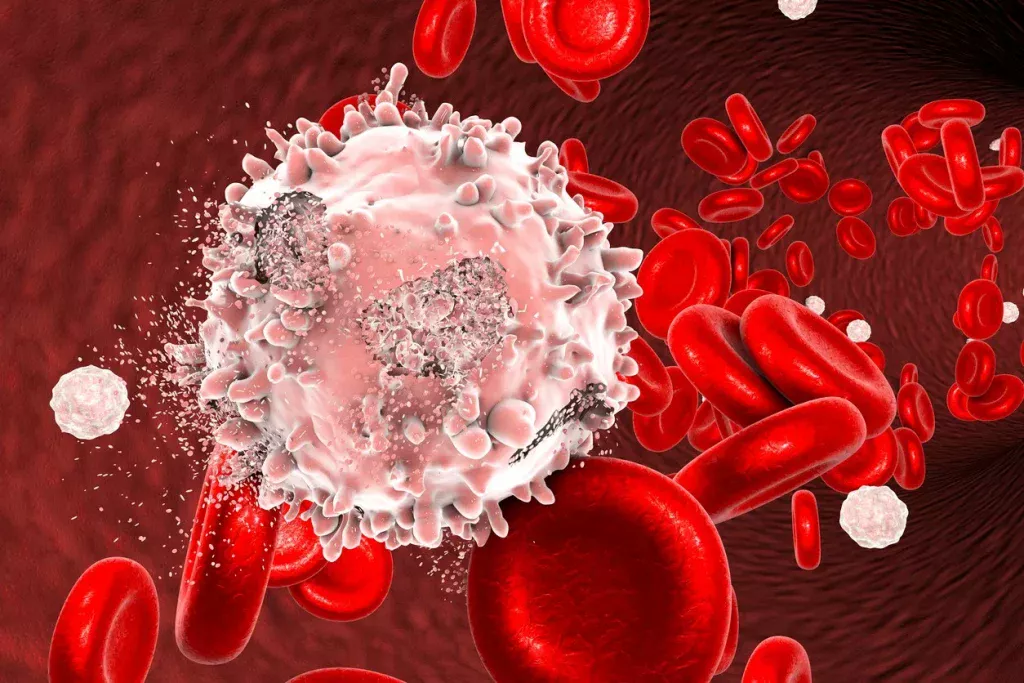
Interessant genoeg hadden de asperigimycines geen effect op borst-, lever- of longkankercellen, wat wijst op een veelbelovende specificiteit die zich zou kunnen vertalen in meer gerichte en minder giftige behandelingen voor de patiënt.
Afgezien van de puntbevinding, opent dit werk een nieuw hoofdstuk in het onderzoek naar schimmelmedicijnen. De onderzoekers hebben al soortgelijke genclusters geïdentificeerd in andere schimmels, wat wijst op onbekend terrein dat nog moet worden verkend. “We hebben nog maar net het oppervlak ontdekt,” zegt Nie. “Elk van deze verbindingen heeft een verhaal te vertellen en potentieel om te onthullen.”
De volgende stap is het testen van de asperigimycines in diermodellen. Als de resultaten standhouden, is het niet onredelijk om na te denken over toekomstige klinische proeven op mensen.